Химические свойства гидроксида натрия. Получение гидроксида натрия
Применение каустической соды в быту обусловлено одним из ее свойств – нейтрализовать жиры и другие органические загрязнения. Именно способность растворять заторы из грязи и органических накоплений помогает справиться с очисткой канализации в частном секторе и многоквартирных домах. Кроме того, едкий натр (каустическая сода, гидроксид натрия, каустик) используется и для приготовления мыла своими руками в домашних условиях.
Очистка сливных труб и канализации
Существует два способа прочистки стока в умывальнике, ванне или душевой кабине, а также туалета или канализационной системы в частном доме. Первый больше подходит для прочистки стоков в системе канализации частного дома, второй – для очищения сифонов и сливных стояков в многоэтажках. Инструкция по применению, 1-й вариант:
- 2 кг каустической соды заливают холодной водой (4 л);
- полученный раствор выливают в канализацию;
- около часа нежелательно сливать воду: в это время едкий натр расщепляет жиры и другую органику.
- по истечении часа заливают воду (12-15 литров) с температурой 85-90 ºC.
При регулярной прочистке канализационных труб таким методом в доме гарантированно не будет неприятного запаха из труб, который появляется благодаря разложению остатков пищи и других биологических веществ. Инструкция по применению, 2-й способ:
- в горловину мойки или ванны засыпается до 150 г каустика;
- далее на порошок осторожно выливается до 2 литров горячей воды;
- через 5-10 минут горячая вода заливается повторно;
- около часа нельзя допускать попадания в горловину воды.
Едкий натр можно использовать после очистки труб кислотными веществами для нейтрализации агрессивного воздействия.

Чистка кастрюль
Так как гидроксид натрия хорошо справляется с жировыми загрязнениями, его используют для , кастрюль и другой кухонной утвари. Стоит сразу заметить, что такое применение не подходит для посуды из алюминия или тефлона. зато эмалированные, чугунные и стальные кастрюли доводит до идеального состояния. Для такой процедуры необходимо:
- в большую металлическую емкость залить воду (не менее 10 литров);
- всыпать туда едкий натр (200 г);
- добавить 1 брусок натертого на крупной терке хозяйственного мыла;
- влить 150 г канцелярского клея (жидкого стекла);
- хорошо размешать все и вложить в полученную смесь посуду;
- довести до кипения и держать на небольшом огне еще 2 часа;
- достать очищенную посуду и хорошо вымыть под проточной водой.
Таким же способом можно бороться с застарелым жиром на тарелках, только время кипячения сокращается до 10 минут.

Мыловарение
Каустик используется еще в одной области — для мыловарения. Его применение является обязательным, так как едкий натр — главный ингредиент в составе мыла:
- каустическая сода;
- растительное масло;
- эфирное масло;
- очищенная (дистиллированная) вода.
Существует множество рецептов мыла, в которых разнятся пропорции и добавляются специфические составляющие (в этом и состоит секрет мыловарения), но, используя основные ингредиенты, можно поэкспериментировать и приготовить мыло своими руками. Для этого каустик соединяют с водой, вводят в раствор растительное и эфирное масло. Смешивают составляющие до получения однородной массы, после чего выливают ее в формочки, где она застывает в течение суток.
Для косметических целей нужен едкий натр с высокой степенью очистки. Его можно приобрести в магазинах для мыловаров.

Хранение каустика и меры предосторожности
Чтобы разобраться, как правильно хранить едкий натр в домашних условиях, нужно выяснить, чем он является. Что такое каустическая сода? Прежде всего, это химическое вещество – сильная щелочь, вызывающая ожоги. Поэтому и раствор, и порошок необходимо держать в местах, недоступных для детей, в плотно закрытой таре с соответствующим ярлыком. Также каустик относится к горючим и взрывоопасным веществам, следовательно, он должен находиться вдали от нагревательных приборов и источников открытого огня.
Каустическую соду хранят в герметичной таре: порошок в бумажных мешках или полиэтиленовых банках, а жидкость в таре из плотного полиэтилена с резиновой пробкой. Срок хранения и жидкости, и гранул – 12 месяцев. Самостоятельно приготовленный 3%-й раствор также может хранится до 12 месяцев, однако перед использованием нужно проверить, не образовался ли осадок. Если в растворе наблюдаются хлопья, возможно, произошло преобразование в карбонат калия и он утратил свои свойства. Прозрачность или непрозрачность тары на свойства каустика никак не влияет.
Работая с гидроксидом натрия, необходимо соблюдать меры предосторожности:
- работать в резиновых перчатках;
- защищать глаза и слизистые оболочки от попадания химического вещества;
- не допускать попадания внутрь.
Если же каустик все же попал на кожу, нужно сразу промыть ее проточной водой. При случайном приеме внутрь или попадании в глаза лучше сразу же обратится к врачу, так как это может вызвать серьезные проблемы со зрением (отмирание тканей роговицы) или ожог гортани и пищевода, а также желудка.

Еще немного разных фактов
Каустик в быту находит применение и для других целей.
- Для дезинфекции в подсобных хозяйствах при опасных инфекционных заболеваниях у скота помещения обрабатывают 4%-м раствором едкого натра. Животных на время обработки выводят.
- При очистке металлической поверхности от ржавчины кислотой каустик является основным ингредиентом для пассивации. После обработки кислотными растворами металл обрабатывают смесью формалина, каустической соды, аммония и воды.
- Для удаления трудновыводимых жировых пятен или пятен от мазута с одежды. Вещи замачиваются 2 часа в воде с добавлением 2%-го раствора гидроксида натрия – 1 ст. ложка на литр воды. После этого стираются обычным способом. Если стирка ручная, обязательно должны надеваться резиновые перчатки.
Внимание!
Способ очистки от пятен каустической содой не походит для шелковых и шерстяных тканей. В 10%-м растворе каустика они растворяются без остатка, но и меньшая концентрация принесет этим тканям ощутимый ущерб.
Введение .
Гидроксид натрия или едкий натр (NaOH), хлор, соляная кислота НС1 и водород получают в промышленности в настоящее время методом электролиза раствора хлорида натрия.
Едкий натр или гидроксид натрия - сильная щелочь, называемая в быту каустической содой, применяется в мыловарении, в производстве глинозема - полупродукта для получения металлического алюминия, в лакокрасочной, нефтеперерабатывающей промышленности, в производстве искусственного шелка, в промышленности органического синтеза и других отраслях народного хозяйства.
При работе с хлором, хлористым водородом, соляной кислотой и едким натром необходимо строго соблюдать правила техники безопасности: вдыхание хлора вызывает резкий кашель и удушье, воспаление слизистых оболочек дыхательных путей, отек легких, а в дальнейшем образование в легких воспалительных очагов.
Хлористый водород даже при незначительном содержании его в воздухе вызывает раздражение в носу и гортани, покалывание в груди, хрипоту и удушье. При хроническом отравлении малыми его концентрациями особенно страдают зубы, эмаль которых быстро разрушается.
Отравления соляной кислотой весьма сходны с отравлениями хлором.
Химические способы получения гидроксида натрия.
К химическим способам получения гидроксида натрия относятся известковый и ферритный.
Известковый способ получения гидроксида натрия заключается во взаимодействии раствора соды с известковым молоком при температуре около 80°С. Этот процесс называется каустификацией; он описывается реакцией
Na 2 C0 3 + Са (ОН) 2 = 2NaOH + CaC0 3 (1)
растворосадок
По реакции (1) получается раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора, который упаривается до получения расплавленного продукта, содержащего около 92% NaOH. Расплавленный NaOH разливают в железные барабаны, где он застывает.
Ферритный способ описывается двумя реакциями:
Na 2 C0 3 + Fe 2 0 3 = Na 2 0 Fe 2 0 3 + C0 2 (2)
феррит натрия
Na 2 0 Fe 2 0 3 -f H 2 0 = 2 NaOH + Fe 2 O 3 (3)
раствор осадок
реакция (2) показывает процесс спекания кальцинированной соды с окисью железа при температуре 1100-1200°С. При этом образуется спек - ферритнатрия и выделяется двуокись углерода. Далее спек обрабатывают (выщелачивают) водой по реакции (3); получается раствор гидроксида натрия и осадок Fe 2 O 3 , который после отделения его от раствора возвращается в процесс. Раствор содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92% NaOH.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество топлива, получаемый едкий натр загрязнен примесями, обслуживание аппаратов трудоемко и др. В настоящее время эти методы почти полностью вытеснены электрохимическим способом производства.
Понятие об электролизе и электрохимических процессах.
Электрохимическими процессами называют химические процессы, протекающие в водных растворах или расплавах под действием постоянного электрического тока.
Растворы и расплавы солей, растворы кислот и щелочей, называемые электролитами, относятся к проводникам второго рода, в которых перенос электрического тока осуществляется ионами. (В проводниках первого рода, например металлах, ток переносится электронами.) При прохождении электрического тока через электролит на электродах происходит разряд ионов и выделяются соответствующие вещества. Этот процесс называется электролизом. Аппарат, в котором осуществляется электролиз, называется электролизером или электролитической ванной.
Электролиз используется для получения ряда химических продуктов- хлора, водорода, кислорода, щелочей и др. Следует отметить, что путем электролиза получают химические продукты высокой степени чистоты, в ряде случаев недостижимой при химических методах их производства.
К недостаткам электрохимических процессов следует отнести высокий расход энергии при электролизе, что увеличивает стоимость получаемых продуктов. В связи с этим проведение электрохимических процессов целесообразно только на базе дешевой электрической энергии.
Сырье для получения гидроксида натрия.
Для производства гидроксида натрия, хлора, водорода используют раствор поваренной соли, который подвергают электролизу Поваренная соль встречается в природе в виде подземных залежей каменной соли, в водах озер и морей и в виде естественных рассолов или растворов. Залежи каменной соли находятся в Донбассе, на Урале, в Сибири, Закавказье и других районах. Богаты солью у нас в стране и некоторые озера.
В летнее время происходит испарение воды с поверхности озер, и поваренная соль выпадает в виде кристаллов. Такая соль называется самосадочной. В морской воде содержится до 35 г/л хлорида натрия. В местах с жарким климатом, где происходит интенсивное испарение воды, образуются концентрированные растворы хлорида натрия, из которых он кристаллизуется. В недрах земли, в пластах соли протекают подземные воды, которые растворяют NaCl и образуют подземные рассолы, выходящие через буровые скважины на поверхность.
Растворы поваренной соли, независимо от пути их получения содержат примеси солей кальция и магния и до того, как они передаются в цеха электролиза, подвергаются очистке от этих солей. Очистка необходима потому, что в процессе электролиза могут образовываться плохо растворимые гидроокиси кальция и магния, которые нарушают нормальный ход электролиза.
Очистка рассолов производится раствором соды и известковым молоком. Помимо химической очистки, растворы освобождаются от механических примесей отстаиванием и фильтрацией.
Электролиз растворов поваренной соли производится в ваннах с твердым железным (стальным) катодом и с диафрагмами и в ваннах с жидким ртутным катодом. В любом случае промышленные электролизеры, применяемые для оборудования современных крупных хлорных цехов, должны иметь высокую производительность, простую конструкцию, быть компактными, работать надежно и устойчиво.
Электролиз растворов хлористого натрия в ваннах со стальным катодом и графитовым анодом .
Дает возможность получать гидроксид натрия, хлор и водород в одном аппарате (электролизере). При прохождении постоянного электрического тока через водный раствор хлорида натрия можно ожидать выделения хлора:
2CI - - 2е Þ С1 2 (а)
а также кислорода:
20Н - - 2е Þ 1/2О 2 + Н 2 О(б)
H 2 0-2eÞ1/2О 2 + 2H +
Нормальный электродный потенциал разряда ОН - -ионов составляет + 0,41 в, а нормальный электродный потенциал разряда ионов хлора равен + 1,36 в. В нейтральном насыщенном растворе хлористого натрия концентрация гидроксильных ионов около 1 ·10 - 7 г-экв/л. При 25° С равновесный потенциал разряда гидроксильных ионов будет
Равновесный потенциал разряда, ионов хлора при концентрации NaCI в растворе 4,6 г-экв/л равен
Следовательно, на аноде с малым перенапряжением должен в первую очередь разряжаться кислород.
Однако на графитовых анодах перенапряжение кислорода много выше перенапряжения хлора и поэтому на них будет происходить в основном разряд ионов С1 - с выделением газообразного хлора по реакции (а).
Выделение хлора облегчается при увеличении концентрации NaCI в растворе вследствие уменьшения при этом величины равновесного потенциала. Это является одной из причин использования при электролизе концентрированных растворов хлорида натрия, содержащих 310-315 г/л.
На катоде в щелочном растворе происходит разряд молекул воды по уравнению
Н 2 0 + е = Н + ОН - (в)
Атомы водорода после рекомбинации выделяются в виде молекулярного водорода
2Н Þ Н 2 (г)
Разряд ионов натрия из водных растворов на твердом катоде невозможен вследствие более высокого потенциала их разряда по сравнению с водородом. Поэтому остающиеся в растворе гидроксид - ионы образуют с ионами натрия раствор щелочи.
Процесс разложения NaCI можно выразить таким образом следующими реакциями:
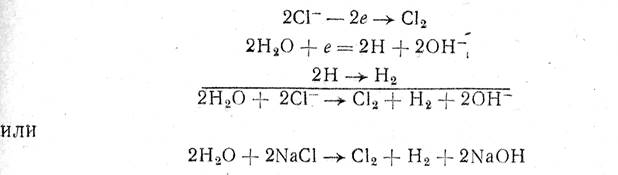
т. е. на аноде идет образование хлора, а у катода - водорода и гидроксида натрия.
При электролизе, наряду с основными, описанными процессами, могут протекать и побочные, один из которых описывается уравнением (б). Помимо этого, хлор, выделяющийся на аноде, частично растворяется в электролите и гидролизуется по реакции
В случае диффузии щелочи (ионов ОН -) к аноду или смещения катодных и анодных продуктов хлорноватистая и соляная кислоты нейтрализуются щелочью с образованием гипохлорита и хлорида натрия:
НОС1 + NaOH = NaOCl + Н 2 0
НС1 + NaOH = NaCl + Н 2 0
Ионы ClO - на аноде легко окисляются в ClO 3 - . Следовательно, из-за побочных процессов при электролизе будут образовываться гипохлорит, хлорид и хлорат натрия, что приведет к снижению выхода по току и коэффициента использования энергии. В щелочной среде облегчается выделение кислорода на аноде, что также будет ухудшать показатели электролиза.
Чтобы уменьшить протекание побочных реакций, следует создать условия, препятствующие смешению катодных и анодных продуктов. К ним относятся разделение катодного и анодного пространств диафрагмой и фильтрация электролита через диафрагму в направлении, противоположном движению ОН - ионов к аноду. Такие диафрагмы называются фильтрующими диафрагмами и выполняются из асбеста.
Повышение температуры электролиза и концентрации NaCl в электролите, благодаря которым уменьшается растворимость хлора, а также снижение концентрации NaOH в католите сокращают вероятность побочных процессов.
Повышение температуры электролиза увеличивает не только выход по току, но и электропроводность электролита, благодаря чему снижается напряжение на ванне. Таким образом, повышение температуры уменьшает расход электрической энергии и поэтому обычно электролиз растворов хлорида натрия проводят при 70-80° С.
Промышленные электролизеры с фильтрующей диафрагмой широко применяются в промышленности. Схема такой ванны приведена на рис. 1 Ванна имеет стальной перфорированный (с отверстием) катод и графитовый анод. К катоду плотно прилегает фильтрующая диафрагма из асбестового картона.
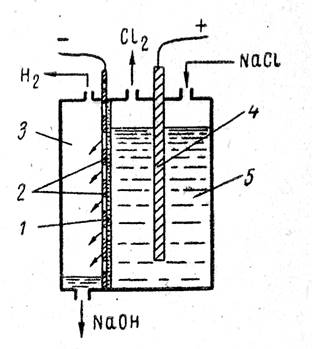 Раствор хлорида натрия подается в анодное пространство, фильтруется сквозь диафрагму и достигает катода. Скорость фильтрации электролита характеризуется так называемой протекаемостью диафрагмы v
(см 3
/ч)
и зависит от площади сечения диафрагмы F
(см 1),
гидростатического давления столба электролита h
,
толщины диафрагмы b (см)
и вязкости электролита μ .
Раствор хлорида натрия подается в анодное пространство, фильтруется сквозь диафрагму и достигает катода. Скорость фильтрации электролита характеризуется так называемой протекаемостью диафрагмы v
(см 3
/ч)
и зависит от площади сечения диафрагмы F
(см 1),
гидростатического давления столба электролита h
,
толщины диафрагмы b (см)
и вязкости электролита μ .
При прохождении постоянного электрического тока на аноде образуется хлор, на катоде - водород и щелочь, которая, проходя через отверстия катода, стекает в катодное пространство и удаляется из ванны.
Схема ванны с фильтрующей диафрагмой:
1- диафрагма; 2 - стальной катод;
3 - катодное пространство;
4 - анод; 5 - анодное пространство
В ваннах не происходит полного разложения поваренной соли и
устанавливается постоянная концентрация щелочи и неразложившейся поваренной соли.
В электролитическом щелоке, вытекающем из ванны, содержится 110-120 г/л NaOH и 180-170 г/л NaCl.
Промышленные электролизеры должны иметь большую производительность, что достигается увеличением нагрузки. Применение катодов с очень развитой поверхностью позволяет создавать компактные электролизеры с нагрузкой до 50000 а. Диафрагма в этом случае насасывается или «осаждается» на поверхность катода из суспензии асбестового волокна в соляно-щелочных растворах при помощи вакуума.

Рис. 2. Ванна с осажденной диафрагмой:
1- бетонное днище; 2 - стальной катод; 3 - бетонная крышка; 4 - труба для подачи рассола; 5 - труба для отвода хлора; 6 - графитовые аноды; 7 - штуцер для удаления водорода; 8 - трубка для слива электролитического щелока; 9 - медный токоведущий
стержень
Примером ванны с осажденной диафрагмой может служить ванна Хукера типа S, рис. 2. Эта ванна состоит из трех основных частей - бетонного днища, стального катода и бетонной крышки. Днище имеет форму прямоугольного корыта, в котором залиты свинцом нижние концы графитовых анодов и медный стержень, служащий для подвода тока. Аноды представляют собой графитовые пластины. Катод - стальная рама, внутри которой смонтирован ряд плоских карманов из стальной сетки. Расположение карманов и их ширина таковы, что установке катода на днище ванны карманы помещаются точно между анодами.
В крышке ванны расположены отверстия для подачи рассола и отвода хлора. Электролизер имеет тепловую изоляцию уменьшающую потери энергии за счет отдачи тепла в окружающую среду.
Электролиз растворов хлорида натрия в ваннах с ртутным катодом и графитовым анодом.
Дает возможность получать более концентрированные продукты, чем в ваннах с диафрагмой.
При пропускании через раствор NaCl постоянного электрического тока на графитовом аноде происходит разряд ионов С1 - с последующим выделением газообразного хлора
2С1 - - 2е Þ С1 2
На ртутном катоде выделение водорода происходит с большим перенапряжением. Если на железном катоде потенциал выделения водорода из нейтрального раствора равен 0,415 в, то на ртутном катоде он составляет 1,7 - 1,85 в. Натрий же на ртути выделяется с большим эффектом деполяризации, обусловленным образованием амальгамы натрия NaHg n , растворяющейся в избытке ртути. Благодаря этому потенциал разряда натрия на ртутном катоде оказывается ниже равновесного, а именно 1,2 в, в то время как его равновесный потенциал равен 2,71 в. Таким образом, на ртутном катоде протекают следующие процессы:
Na + + е Þ Na
Na + n Н g = NaHg n
и водород практически почти не выделяется.
Амальгама натрия разлагается в специальном аппарате - разлагателе водой по реакции
NaHg n + Н 2 0 = NaOH + 1/2Н 2 + nHg
Электролиз в ванне с ртутным катодом протекает в среднем при напряжении 4,3-4,4 в.
Ванна с ртутным катодом, принципиальная схема которой приведена на рис. 3, состоит из двух частей: электролизера и разлагателя.
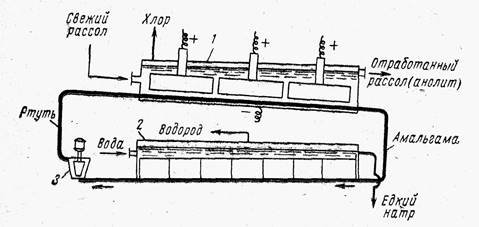 Электролизер и разлагатель конструктивно могут быть разделены и сообщаться друг с другом трубопроводом или могут быть расположены в одном общем кожухе.
Электролизер и разлагатель конструктивно могут быть разделены и сообщаться друг с другом трубопроводом или могут быть расположены в одном общем кожухе.
В любом случае электролизер - длинный ящик прямоугольного сечения, сверху закрытый крышкой, в которой укреплены графитовые аноды. Рис. 3. Схема ванны с ртутным катодом:
1- электролизер; 2 - разлагатель; 3 - насос
К слегка наклонному дну ванны подведена катодная шина и по нему непрерывно движется тонкий слой ртути. Таким образом, днище ванны является катодом. Электролизер питается концентрированным (310-315 г/л) раствором хлорида натрия, который в процессе электролиза обедняется поваренной солью до концентрации 260-270 г/л, выводится из ванны, обесхлоривается под разряжением и при продувке его сжатым воздухом, донасыщается солью, очищается от примесей (в схеме не показано) и передается обратно на электролиз. Образующийся хлор выводится через крышку ванны.
При движении ртути по дну электролизера в процессе электролиза получается амальгама натрия, которая растворяется в ртути и выводится из электролизера в разлагатель. Разлагатели могут быть различной конструкции - горизонтальные и вертикальные. Горизонтальные разлагатели представляют собой прямоугольный желоб, закрытый крышкой. В разлагатель поступает вода и из него отводятся образующиеся продукты - водород и щелочь. Дно разлагателя имеет небольшой уклон, благодаря чему ртуть движется по дну, выводится из разлагателя и подъемниками различного типа передается в электролизер.
Ванна с ртутным катодом занимает большие площади, что связано с горизонтальным расположением ртутного катода. Существуют ванны, в которых катодами служат вертикальные амальгамированные диски. Эти ванны компактны, но сложны конструктивно и в эксплуатации.
Сопоставление основных показателей работы ванн двух типов показывает, что вследствие высокого напряжения на ваннах с ртутным катодом расход энергии выше, чем в диафрагменных. Кроме того, эксплуатация ванн с ртутным катодом более сложна, чем диафрагменных, капитальные затраты на их установку выше и условия труда в цехах, оборудованных ртутными ваннами, тяжелее, чем в цехах, где установлены ванны с диафрагмой.
Возможность получения в ртутных ваннах концентрированных щелоков, свободных от поваренной соли, является существенным достоинством ртутных ванн. Исходя из этого во всех случаях, когда требуется чистая щелочь (например, для производства вискозного волокна), предпочтение должно быть отдано ваннам с ртутным катодом. В связи с ростом потребности в чистом каустике электролиз в ваннах с ртутным катодом приобрел большое распространение.
Щелочь, получаемая при электролизе, в виде растворов, подвергается концентрированию в выпарных аппаратах. Щелочь из диафрагменных ванн содержит до 130- 140 г/л NaOH и 180-170 г/л NaCl. Растворимость поваренной соли с увеличением концентрации NaOH в растворе падает. Так, в щелоке, содержащем 50% (769 г/л) NaOH, при 20° С растворимость NaCl составляет 13,9 г/л. Вследствие этого при выпарке электролитических щелоков, полученных в ваннах с диафрагмой, наряду с концентрированием раствора происходит кристаллизация хлорида натрия, который возвращается на электролиз. Практически после упарки и плавки получают щелочь, содержащую 92-94% NaOH, 2-3% NaCl.
Вывод.
Таким образом гидроксид натрия на сегодняшний день получают методом электролиза водного раствора хлорида натрия. При этом используются два вида электролизеров, каждый из которых имеет свои достоинства и недостатки. Но в обоих случаях процесс получения гидроксида натрия сопровождается получением газообразных побочных продуктов, которые являются опасными веществами как для человека так и для окружающей среды. Поэтому следует соблюдать особые меры безопасности на данном производстве.
Литература.
1. Общая химическая технология. Под ред. И.П. Мухленова. Учебник для химико-технологических специальностей вузов. М.: Высшая школа.
2. Фурмер И.Э., Зайцев В.Н. Общая химическая технология. – М.: Высшая школа, 1978.
(каустическая сода) представляет собой твердое белое вещество, имеющее вид гранул или плавленой массы, обладающее гигроскопическими свойствами. При растворении имеет свойство выделять тепло. За счет сильного разрушительного действия на ткани, кожу и прочие органические вещества каустическая сода (формула NaOH) имеет название "едкая щелочь" или "едкий натрий", а на производственных предприятиях - "каустик". В жидком состоянии, как правило, окрашенная или бесцветная жидкость, в которой может образовываться осадок.
Каустическая сода: применение
Соду каустическую (натрий едкий) используют для бытовых нужд, а также в разных отраслях промышленности. Это самая распространенная щелочь.
Каустическая сода применение нашла в следующих сферах:
- каустическая сода - зарегистрированная пищевая добавка Е524, которая используется для производства мороженого, шоколада, различных напитков, как размягчающее средство для маслин и др.
- в целлюлозно-бумажной промышленности (изготовление картона, разных видов бумаги, плит из древесного волокна, искусственного волокна и многого другого);
- для производства биодизельного топлива, которое изготовляется из растительных масел;
- в химической промышленности (для изготовления моющих средств, нейтрализации окислов и кислот, для титрования алюминия, для производства масел и прочего);
- в легкой промышленности (для отбеливания тканей, в производстве шелка);
- в автомобильном производстве (используют в изготовлении щелочных аккумуляторов);
- в пищевой промышленности (для промывки оборудования; обработки и производства продуктов питания).
Производство каустической соды
Самый распространенный способ получения едкого натрия - электролиз водного раствора галита (NaCL). Химическая реакция проходит с сопровождением выделения водорода и хлора.
Часто каустическая сода производится путем электролиза с использованием полимерных или асбестовых катодов (мембранные и диафрагменные методы), более редко получают путем электролиза с ртутным катодом.
К самому удобному методу относится ртутный способ производства, где катод - это металлическая ртуть.
При помощи высокого коэффициента перенапряжения на ртути водорода ионы натрия у катода разряжаются, и в итоге получается амальгама натрия, которая разлагается в горячей воде. В результате получается очень чистый NaOH, потому как в нем отсутствуют примеси. Однако этот метод считается очень вредным, поскольку применение металлической ртути вызывает загрязнение окружающей среды.
Мембранный и диафрагменный методы являются более эффективными, не требующими больших затрат. Именно их чаще всего применяют во всем мире.

Упаковка продукта
Каустическая сода, в зависимости от ее вида, может быть упакована различными способами. В твердом состоянии ее компонуют в стальные барабаны. Раствор каустической соды заливают в специальные автомобильные контейнеры и железнодорожные цистерны.

Хранение вещества
Жидкую соду хранят в помещениях в закрытых емкостях, устойчивых к действию щелочей. Твердый едкий натрий хранится в упакованном виде в закрытых неотапливаемых складах.
Транспортировка
Перевозят каустическую соду при помощи транспорта (железнодорожного, автомобильного и водного). При проведении доставки твердого едкого натрия данный продукт упаковывают в мешки, а жидкое вещество перевозят в специальных железнодорожных цистернах и емкостях. При транспортировке каустической соды следует избегать нагревания и попадания на нее влаги.
Гарантийный срок хранения едкого натрия с даты изготовления - 1 год.

Описание
В мире добывается и используется в течение года более 58 млн. тонн каустической соды. Данное вещество имеет удельный вес 2,13, может хорошо растворяться в воде (при температуре 0 градусов - 43%), но не растворимо в дихлорэтане. Натрий едкий идет на изготовление дегазирующего раствора №2, кроме того, вещество используют для дегазации местности. Аммиачно-щелочной раствор №2 состоит из таких компонентов:
- натрия едкого (2%);
- аммиака (20%);
- моноэтаноламина (5%).
Данным раствором проводят дегазацию боевой техники, военного транспорта, разного вооружения, которые оказались заражены такими отравляющими веществами, как, например, зарин.
Аммиак и моноэтаноламин используют как дегазирующие вещества, а также для снижения температуры замерзания состава до - 40°C. Данный раствор хранят в железных бочках, объем которых - 100 и 250 л, в них и происходит транспортировка в расположение воинских частей и на производства.
Концентрированный раствор способен разрушать обувь и ткани, а также разъедать кожу людей.
Меры предосторожности
При обращении с данным веществом нельзя забывать об опасности, которую оно может в себе содержать. Каустическая сода (формула NaOH) едкая, коррозионно активная, относится ко 2 классу опасности. При работе с ней нужно обязательно соблюдать все необходимые меры предосторожности. Попадание вещества в глаза или на кожу может вызвать серьезный химический ожог.
При попадании натрия едкого на слизистую поверхность нужно немедленно пораженный участок промыть проточной водой, а в случае попадания на кожу протереть раствором уксусной кислоты.
- брызгозащитные химические очки (для защиты глаз);
- резиновые перчатки (для защиты рук);
- прорезиненный костюм или спецодежду, пропитанную винилом (для защиты туловища).
Применение каустической соды осуществляется во многих областях производства и даже в быту, но чем является эта сода и чем она так полезна?
Что такое каустическая сода?
Каустическая сода – одна из самых известных, распространенных и сильных щелочей. Химическая формула которой — NaOH.
Помимо выше упомянутых, данное вещество также имеет такие наименования: каустик, гидроксид натрия, едкая щелочь или едкий натр. Сам гидроксид представлен чешуйчатыми гранулами белого цвета, не имеющие никакого запаха. Размер чешуек может достигать 0,5 мм.
Полезные свойства каустической соды

Вещество владеет отличными гигроскопическими свойствами, и оно довольно хорошо растворяется в жидкости. Во время растворения начинает выделяться тепло. Щелочь легко переносит абсолютно любые виды перевозки. Это зависит от агрегатного состояния. В жидком используют цистерны, в твердом на помощь приходят мешки.
Каустик занял устойчивое положение сразу во многих отраслях: медицинская, химическая, металлургическая, автомобильная, пищевая, легкая, газовая, нефтяная.
Вещество принимают во многих областях промышленности, но, несмотря на это, оно имеет и отрицательные свойства. К недостаткам можно отнести:
- Щелочь едкая, нужно обязательно использовать защитные средства;
- Нужно быть внимательным и следить за работой, ведь каустик способен разъедать эмаль ванны.
Но все равно сода имеет немало положительных сторон:

- Стопроцентное разъедание жировых, а также органических отложений;
- Даже после того, как ей промоют канализации, щелочь будет действовать;
- Легко сглаживает любые шероховатости на трубах, что замедлит отложение;
- Достаточно использования лишь раз в месяц;
- Низкая цена и доступность.
- Вещество обладает сильными разрушительными свойствами, способно разъедать цинк и алюминий. Соду применяют в процессе производственной дезинфекции. Едкий натр взрывоопасен, его горючесть относят к повышенной опасности.
Некоторые другие свойства каустической соды
- В ацетоне и эфирах абсолютно не растворим;
- Высокая растворимость в спиртовых растворах глицерина, этанола и метанола;
- Вещество негорючее, температура плавления — триста восемнадцать градусов Цельсия;
- Кипит при температуре тысяча триста девяносто градусов Цельсия;
- Опаснейшее свойство каустика заключается в его резкой и бурной реакции при контактировании с металлами алюминия, свинца, цинка и олова;
- Является сильным основанием, из-за чего способно образовывать взрывоопасный легкогорючий газ;
- Опасность возгорания возникает при контакте едкого натра с аммиаком;
- В расплавленном состоянии способно разрушать стекло и фарфор.
Применение в быту в домашних условиях

Техника безопасности
Гидроксид натрия — мощнейший щелочной раствор, способный легко разъедать почти любые покрытия. При использовании соды, следует соблюдать правила, которые могут помочь сохранить здоровье. При небрежном обращении с щелочью она может попасть на кожу и разъесть ее, образуется экзема или язва. Сода, попавшая в глаза или слизистые ротовой полости, также таит в себе большую опасность. Вещество отлично впитывает жидкость и начинает выделение тепла, и в таком случае ожога уже не получится избежать. Чтобы такого не происходило, нужно стараться придерживаться правил в обращении с каустиком.
Инструкция по применению

 Любое опасное средство обязательно нуждается в аккуратном и тщательном обращении, каустическая сода тоже попадает под их категорию. При покупке смеси каустической соды серьезно и важно и необходимо изучить абсолютно все нужные рекомендации по применению и обязательно ее соблюдать. Тогда даже такое небезопасное вещество, как каустик, окажет помощь при домашних делах и не навредит жизни и здоровью.
Любое опасное средство обязательно нуждается в аккуратном и тщательном обращении, каустическая сода тоже попадает под их категорию. При покупке смеси каустической соды серьезно и важно и необходимо изучить абсолютно все нужные рекомендации по применению и обязательно ее соблюдать. Тогда даже такое небезопасное вещество, как каустик, окажет помощь при домашних делах и не навредит жизни и здоровью.
Пропорции
При выварке чугуна и стали для того, чтобы удалить смолистые отложения, для снятия старой краски с автомобилей, для выварки рам требуется смесь каустика концентрацией от пятидесяти до ста грамм на литр или более. Для того чтобы обезжирить алюминий, требуются растворы кальцинированного гидроксида натрия двадцать пять — тридцать грамм на литр, тринатрийфосфата двадцать пять — тридцать грамм на литр, а также жидкого стекла десять — пятнадцать грамм на литр.
При этом температура всегда держится от 80 градусов Цельсия.
Обширное использование в быту

Несмотря на всю небезопасность, едкая щелочь повсюду применяется людьми в быту. Используется в качестве растворителя для чистки труб и посуды, для варки мыла и бывает в садоводстве.
Время хранения гидроксида натрия - один год с даты выпуска производителем. После истечения срока раствор частично теряет свои свойства, а это означает, что его дальнейшее использование уже не сможет принести желаемого итога. Хранить каустик желательно в плотно закрытом сосуде, в темном и прохладном месте.
Сброс накипи или жира
Ни в коем случае не следует очищать таким способом алюминиевые или тефлоновые изделия, ведь посуда будет испорчена веществом. Для того, чтобы очистить от накипи посуду, нужно смешать соду с каким угодно порошком, разбавить водой, но, не делая сильно жидким, и нанести на место загрязнения на тридцать минут. После чего начисто промыть и накипь сойдет.
Применение для чистки канализации

Каустическая сода к тому же хорошо применяется не только в домашнем быту, но и на предприятиях. Для удовлетворения некоторых потребностей нужны различные растворы. Чаще всего задаваемый вопрос: как же нужно разводить каустическую соду для получения качественного результата при применении?
Каустиком чистят канализации, ведь раствор способен эффективно и легко разъедать жировые и белковые отложения на трубах. Для того, чтобы очистить поверхность труб с помощью едкой щелочи можно просто купить химический раствор, в составе которого находится сама сода, а затем залить в сливное отверстие.
Некоторые другие варианты, с помощью которых можно прочистить канализацию:
- Соду и уксус можно применить и в другом способе. Необходимо в трубу залить по сто двадцать пять грамм уксуса, и засыпать каустик. Через некоторые время начнется бурная реакция, и какое-то время будет выделяться довольно большое количество пены. Из-за этого слив рекомендуется крепко запечатать пробкой на пару часов. Когда время пройдет, следует в сливное отверстие залить кипяток. Этот способ более чем эффективен для снятия отложений с поверхности труб.
- Есть также и другой не менее эффективный способ чистки труб. Нужно семь литров воды смешать с четырьмя килограммами каустической соды. Затем все старательно перемешать и получившуюся смесь залить в отверстие для слива.
- От засоров в трубах можно избавиться и так: засыпать в слив три ложки вещества, сверху залить двести пятьдесят грамм кипятка. Затем, как и в первом способе следует подождать два-три часа. После того, как реакция закончится, нужно обильно промыть сток водой.
Варка мыла
Мыло ручного приготовления, продающееся в магазинах, стоит немалых денег.
Мыльную продукцию можно изготовить и своими руками, для этого потребуется:

- гидроксид натрия;
- масло;
- вода чистая;
- масла, для достижения аромата.
Сам процесс мыловарения очень прост, но для этого требуется огромная точность и аккуратность в соблюдении всех соотношений. Сода должна быть тщательно разведена и перемешана в воде. Затем на водяной бане следует разогреть масло и налить его в щелочной раствор. После этого должна получиться вязкая и клейкая смесь. Добавляете две-три капель эфирного масла, из-за чего появляется аромат. Полученный результат разложить по заготовленным формочкам и после двадцати четырех часов уже будет можно уже пользоваться мылом изготовленным собственноручно.
Моющие средства
Сейчас в состав абсолютно всех современных стиральных порошков всегда входит каустическая сода. А значит, что можно использовать каустик отдельно во время стирки. В стиральную машину нужно засыпать от трех до пяти ложек соды, количество зависит от того, насколько грязная одежда. Стирка должна идти при температуре от пятидесяти до ста градусов Цельсия. К тому же, соду можно и пользовать при ручной стирке. Это сэкономит порошок и легко уберет любые загрязнения. На десять литров воды надбавляются три столовых ложки каустической соды. Во время процесса замачивания, желательно выдержать белье два часа в щелочном растворе.

Едкий натр также может помочь хорошо вымыть полы. Поначалу следует изготовить раствор: три столовых ложки на пять литров теплой воды. Полы при таком способе моются самим щелочным раствором. Затем, уже после каустического раствора, пол моют обычной водой и старательно вытереть. Если использовать такое вещество, то легко получится не только избавиться от грязи, но к тому же качественно и эффективно продезинфицировать полы в помещении.
Следовательно, каустик часто применяется и в быту в домашних условиях. Вещество несет очень большую опасность, но его разумное использование сделает довольно много полезных вещей и придет на помощь при решении немалого количества бытовых трудностей и вопросов.
Чистка канализации из пластиковых труб
В домашних условиях можно просто сделать средство для чистки пластиковых труб, используя вещи, находящиеся под рукой, соду и порошок для стирки. Сода лучше подействует и поможет, если смешать раствор из каустика и уксуса.
- Сначала следует засыпать в проточину три или четыре столовых ложки каустической соды, залить сверху уксусом и крепко закрыть слив пробкой.
- Снимаете распылитель с душа и вставляете душевой шланг в отверстие.
- Закрываете оставшееся свободное пространство полотенцем или тряпкой, включаете душ на максимальный напор и усиленно промываете слив.
Если это не принесло нужных результатов, то есть еще способ устранения засора вручную:

Для чистки выгребной ямы
Очищение выгребной ямы каустиком очень эффективно и результативно. Но для достижения итога обязательно нужно соблюдать все необходимые правила использования.
К примеру, вы понимаете, что химически бурные вещества могут не только бороться с неприятными запахами, имеющимися у отходов, но и неблагоприятно повлиять на грунт.
Понимая это, злоупотреблять каустиком особо не следует.
Некоторые люди, опробовавшие гидроксид натрия в этом деле, сообщали, что данная щелочь может негативно повлиять не только на землю, но и на человека или животных.
Одним из самых главных и важных правил безопасности во время очистки выгребной ямы каустиком, является доведение ямы до полной герметичности.
Иначе, в противном случае, появляется угроза появления насекомых, разносящих заразу и заболевания за границу септика.
Ни в коем случае нельзя забывать и о скоплении газов, ведь в большом объеме они становятся взрывоопасными, то есть, нужно сделать систему вентиляции, работающую бесперебойно.
Перед всеми процедурами необходимо развести раствор гидроксида натрия в воде.
Можно переходить к последовательности действий.
Для этого нужно:

- десятилитровое пластиковое ведро;
- маленькая лопата или совок;
- перчатки из резины;
- маска и очки.
Каустическая сода не высыпается в яму в состоянии порошка, а выливается уже заранее растворенная в воде.
Вначале при помощи совка или лопатки в ведро наливается от двух до четырех килограмм воды, количество зависит от объема самой ямы.
Затем, в порошок заливается семь-восемь литров воды и тщательно перемешивается. При растворении начинает выделяться тепло, которое немного позже дойдет до шестидесяти градусов Цельсия.
По прошествии времени, уже после растворения соды, полученную массу выливают в сточную яму, обязательно при этом находясь во всех возможных средствах защиты: очках и перчатках.
Активное действие смеси составляет четыре минуты, по количеству циклов, их должно быть два.
Никогда не стоит забывать о приспособлениях защиты. Если щелочь попадет на кожу, то появятся химические ожоги, при более продолжительном контакте кожи с раствором, могут появиться язвы или экземы. Если все-таки средство попадет на кожу, то нужно незамедлительно промыть место ранения обильной струей воды, а затем двухпроцентным раствором борной кислоты.
При поражении глаз, следует незамедлительно промыть их теплой водой в течение пяти минут.
При любых признаках раздражения кожи, следует обратиться к врачу.
Применение каустической соды в пищевой промышленности

В пищевой промышленности каустик известен в качестве дополнения к пище – регулятора Е-524. Широко используется во время производства карамели и мороженого, а также еще некоторых продуктов, вроде лимонада или какао. Каустическая сода принимает участие и в процессе выпечки хлебобулочных изделий и сдоб для достижения более пухлой консистенции, а если обработать изделия раствором едкого щелочи перед началом выпечки, то хлеб приобретет хрустящую румяную корку. Соду используют уместно и разумно при получении максимально нежной и мягкой консистенции различных продуктов питания. Например, рыбу вымачивают в гидроксиде натрия, чтобы получить специальную желеобразную массу, которая принимает участие в готовке блюда лютефиск. Существует такой факт: для размягчения маслин и окраса их в темный цвет также используется каустическая сода.
Где купить?
В настоящее время купить гидроксид натрия можно практически в любом удобном месте. Есть возможность купить едкий натр в розницу в специализированных для таких товаров магазинах. К тому же едкая щелочь продается оптом, что выгодно для промышленных центров.
Как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разьедать кожу, бумагу, стекло и вызывать сильные ожоги. До XVII века, щёлочью (фр. alkali ) называли также карбонаты натрия и калия. В французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия - кальцинированной содой (по растению Salsola Soda, из золы которого её добывали), а карбонат калия - поташем . В настоящее время содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium - калий.
Физические свойства
Гидроксид натрия
Термодинамика растворов
ΔH 0 растворения для бесконечно разбавленного водного раствора -44,45 кДж/моль.
Из водных растворов при 12,3 - 61,8 °C кристаллизуется моногидрат (сингония ромбическая), температура плавления 65,1 °C; плотность 1,829 г/см³; ΔH 0 обр −734,96 кДж/моль), в интервале от -28 до -24°С - гептагидрат, от -24 до -17,7°С - пентагидрат, от -17,7 до -5,4°С -тетрагидрат (α-модификация), от -5,4 до 12,3 °C. Растворимость в метаноле 23,6 г/л (t=28 °C), в этаноле 14,7 г/л (t=28 °C). NaOH·3,5Н 2 О (температура плавления 15,5 °C);
Химические свойства
(в целом такую реакцию можно представить простым ионным уравнением, реакция протекает с выделением тепла (экзотермическая реакция): OH - + H 3 O + → 2H 2 O. )
- с амфотерными оксидами которые обладают как основными, так и кислотными свойствами, и способностью реагировать с щелочами, как с твердыми при сплавлении:
ZnO + 2NaOH → Na 2 ZnO 2 + H 2 O
так и с растворами:
ZnO + 2NaOH (раствор) + H 2 O → Na 2 (раствор) +H 2
(Образующийся анион называется тетрагидроксоцинкат-ионом, а соль, которую можно выделить из раствора - тетрагидроксоцинкатом натрия. В аналогичные реакции гидроксид натрия вступает и c другими амфотерными оксидами.)
- с кислотными оксидами - с образованием солей; это свойство используется для очистки промышленных выбросов от кислотных газов (например: CO 2 , SO 2 и H 2 S):
2Na + + 2OH - + Cu 2+ + SO 4 2- → Cu(OH) 2 ↓+ Na 2 SO 4
Гидроксид натрия используется для осаждения гидроксидов металлов. К примеру, так получают гелеобразный гидроксид алюминия , действуя гидроксидом натрия на сульфат алюминия в водном растворе. Его и используют, в частности, для очистки воды от мелких взвесей.
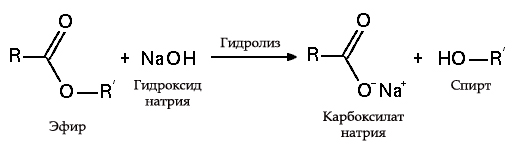
Гидролиз эфиров
- с жирами (омыление), такая реакция необратима, так как получающаяся кислота со щёлочью образует мыло и глицерин . Глицерин впоследствии извлекается из подмыльных щёлоков путем вакуум-выпарки и дополнительной дистилляционной очистки полученных продуктов. Этот способ получения мыла был известен на Ближнем Востоке с VII века:
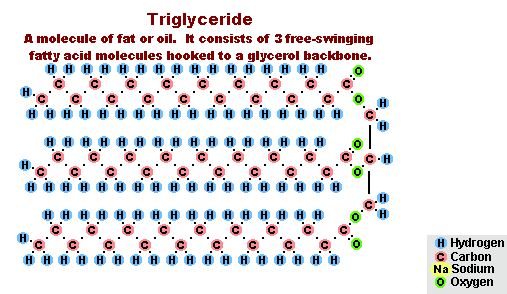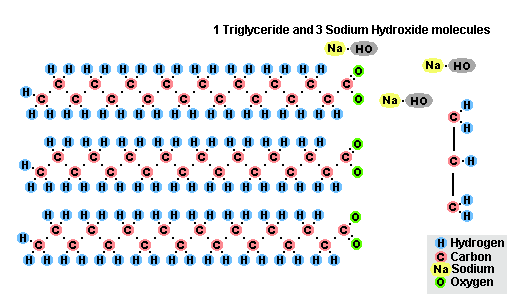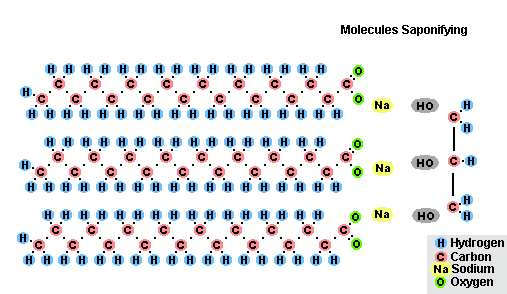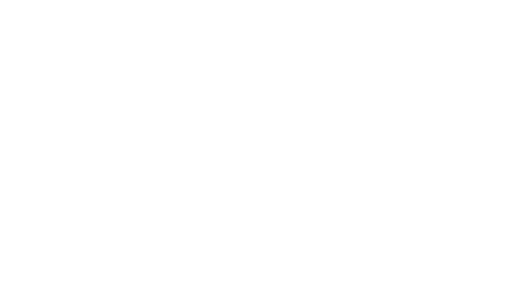
Процесс омыления жиров
В результате взаимодействия жиров с гидроксидом натрия получают твёрдые мыла (они используются для производства кускового мыла), а с гидроксидом калия либо твёрдые, либо жидкие мыла, в зависимости от состава жира.
HO-CH 2 -CH 2 ОН + 2NaOH → NaO-CH 2 -CH 2 -ONa + 2Н 2 O
2NaCl + 2H 2 О = H 2 + Cl 2 + 2NaOH,В настоящее время едкая щёлочь и хлор вырабатываются тремя электрохимическими методами. Два из них - электролиз с твёрдым асбестовым или полимерным катодом (диафрагменный и мембранный методы производства), третий - электролиз с жидким катодом (ртутный метод производства). В ряду электрохимических методов производства самым лёгким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, наименее энергоёмкий и наиболее экологичный, но и самый капризный, в частности, требует сырьё более высокой чистоты.
Едкие щёлочи, полученные при электролизе с жидким ртутным катодом, значительно чище полученных диафрагменным способом. Для некоторых производств это важно. Так, в производстве искусственных волокон можно применять только каустик, полученный при электролизе с жидким ртутным катодом. В мировой практике используются все три метода получения хлора и каустика, при явной тенденции в сторону увеличения доли мембранного электролиза. В России приблизительно 35 % от всего выпускаемого каустика вырабатывается электролизом с ртутным катодом и 65 % - электролизом с твёрдым катодом (диафрагменный и мембранный методы).
Эффективность процесса производства рассчитывается не только по выходу едкого натра, но и по выходу хлора и водорода, получаемых при электролизе, соотношение хлора и гидроксида натрия на выходе 100/110, реакция протекает в следующих соотношениях:
1,8 NaCl + 0, 5 H 2 O + 2,8 МДж = 1,00 Cl 2 + 1,10 NaOH + 0,03 H 2 ,Основные показатели различных методов производства даны в таблице:
| Показатель на 1 тонну NaOH | Ртутный метод | Диафрагменный метод | Мембранный метод |
|---|---|---|---|
| Выход хлора % | 97 | 96 | 98,5 |
| Электроэнергия (кВт·ч) | 3 150 | 3 260 | 2 520 |
| Концентрация NaOH | 50 | 12 | 35 |
| Чистота хлора | 99,2 | 98 | 99,3 |
| Чистота водорода | 99,9 | 99,9 | 99,9 |
| Массовая доля O 2 в хлоре, % | 0,1 | 1-2 | 0,3 |
| Массовая доля Cl - в NaOH, % | 0,003 | 1-1,2 | 0,005 |
Технологическая схема электролиза с твёрдым катодом
Диафрагменный метод - Полость электролизёра с твёрдым катодом разделена пористой перегородкой - диафрагмой - на катодное и анодное пространство, где соответственно размещены катод и анод электролизёра. Поэтому такой электролизёр часто называют диафрагменным, а метод получения - диафрагменным электролизом . В анодное пространство диафрагменного электролизёра непрерывно поступает поток насыщенного анолита. В результате электрохимического процесса на аноде за счет разложения галита выделяется хлор, а на катоде за счет разложения воды - водород. Хлор и водород выводятся из электролизёра раздельно, не смешиваясь:
2Cl - − 2е = Cl 2 0 , H 2 O − 2e − 1/2 О 2 = H 2 .
При этом прикатодная зона обогащается гидроксидом натрия. Раствор из прикатодной зоны, называемый электролитическим щёлоком , содержащий неразложившийся анолит и гидроксид натрия, непрерывно выводится из электролизёра. На следующей стадии электролитический щёлок упаривают и доводят содержание в нём NaOH до 42-50 % в соответствии со стандартом. Галит и сульфат натрия при повышении концентрации гидроксида натрия выпадают в осадок. Раствор едкой щёлочи декантируют от осадка и передают в качестве готового продукта на склад или на стадию упаривания для получения твёрдого продукта, с последующим плавлением, чешуированием или грануляцией. Кристаллический галит (обратную соль) возвращают на электролиз, приготавливая из неё так называемый обратный рассол. Из него во избежание накапливания сульфата в растворах перед приготовлением обратного рассола извлекают сульфат. Убыль анолита возмещают добавкой свежего рассола, получаемого подземным выщелачиванием соляных пластов или растворением твёрдого галита. Свежий рассол перед смешиванием его с обратным рассолом очищают от механических взвесей и значительной части ионов кальция и магния. Полученный хлор отделяется от паров воды, компримируется и подаётся либо на производство хлорсодержащих продуктов, либо на сжижение.
Мембранный метод - аналогичен диафрагменному, но анодное и катодное пространства разделены катионообменной мембраной. Мембранный электролиз обеспечивает получение наиболее чистого каустика.
Технологическая схема электролиза .Основная технологическая стадия - электролиз, основной аппарат - электролитическая ванна, которая состоит из электролизёра, разлагателя и ртутного насоса, объединенных между собой коммуникациями. В электролитической ванне под действием ртутного насоса циркулирует ртуть, проходя через электролизёр и разлагатель. Катодом электролизёра служит поток ртути. Аноды - графитовые или малоизнашивающиеся. Вместе с ртутью через электролизёр непрерывно течёт поток анолита - раствор галита. В результате электрохимического разложения галита на аноде образуются ионы Cl - и выделяется хлор:
2 Cl - - 2е = Cl 2 0 ,
который отводится из электролизёра, а на ртутном катоде образуется слабый раствор натрия в ртути, так называемая амальгама :
Na + + е = Na 0 nNa + + nHg - = Na + HgАмальгама непрерывно перетекает из электролизёра в разлагатель. В разлагатель также непрерывно подаётся хорошо очищенная от примесей вода. В нем амальгама натрия в результате самопроизвольного электрохимического процесса почти полностью разлагается водой с образованием ртути, раствора каустика и водорода:
Na + Hg + Н 2 0 = NaOH + 1/2Н 2 + HgПолученный таким образом раствор каустика, являющийся товарным продуктом, не содержит примеси галита, вредной в производстве вискозы. Ртуть почти полностью освобождается от амальгамы натрия и возвращается в электролизер. Водород отводится на очистку. Анолит, выходящий из электролизера, донасыщают свежим галитом, извлекают из него примеси, внесенные с ним, а также вымываемые из анодов и конструкционных материалов, и возвращают на электролиз. Перед донасыщением из анолита извлекают двух- или трёхступенчатым процессом растворённый в нём хлор.
Лабораторные способы получения
В лаборатории гидроксид натрия получают химическими способами, которые имеют больше историческое, чем практическое значение.
Известковый способ получения гидроксида натрия заключается во взаимодействии раствора соды с известковым молоком при температуре около 80 °C . Этот процесс называется каустификацией; он описывается реакцией:
Na 2 C0 3 + Са (ОН) 2 = 2NaOH + CaC0 3В результате реакции образуется раствор гидроксида натрия и осадок карбоната кальция. Карбонат кальция отделяется от раствора, который упаривается до получения расплавленного продукта, содержащего около 92 % NaOH. Расплавленный NaOH разливают в железные барабаны, где он застывает.
Ферритный способ описывается двумя реакциями:
Na 2 C0 3 + Fe 2 0 3 = Na 2 0 Fe 2 0 3 + C0 2 (1) Na 2 0 Fe 2 0 3 -f H 2 0 = 2 NaOH + Fe 2 O 3 (2)(1) - процесс спекания кальцинированной соды с окисью железа при температуре 1100-1200°С. При этом образуется спек-феррит натрия и выделяется двуокись углерода. Далее спек обрабатывают (выщелачивают) водой по реакции (2); получается раствор гидроксида натрия и осадок Fe 2 O 3 , который после отделения его от раствора возвращается в процесс. Раствор содержит около 400 г/л NaOH. Его упаривают до получения продукта, содержащего около 92 % NaOH.
Химические методы получения гидроксида натрия имеют существенные недостатки: расходуется большое количество топлива, получаемый едкий натр загрязнен примесями, обслуживание аппаратов трудоемко. В настоящее время эти методы почти полностью вытеснены электрохимическим способом производства.
Рынок каустической соды
Мировое производство натра едкого, 2005 год| Производитель | Обьем производства, млн.тонн | Доля в мировом производстве |
|---|---|---|
| DOW | 6.363 | 11.1 |
| Occidental Chemical Company | 2.552 | 4.4 |
| Formosa Plastics | 2.016 | 3.5 |
| PPG | 1.684 | 2.9 |
| Bayer | 1.507 | 2.6 |
| Akzo Nobel | 1.157 | 2.0 |
| Tosoh | 1.110 | 1.9 |
| Arkema | 1.049 | 1.8 |
| Olin | 0.970 | 1.7 |
| Россия | 1.290 | 2.24 |
| Китай | 9.138 | 15.88 |
| Другие | 27.559 | 47,87 |
| Всего: | 57,541 | 100 |
ТР - твердый ртутный (чешуированный);
ТД - твердый диафрагменный (плавленый);
РР - раствор ртутный;
РХ - раствор химический;
РД - раствор диафрагменный.
| Наименование показателя | ТР ОКП 21 3211 0400 | ТД ОКП 21 3212 0200 | РР ОКП 21 3211 0100 | РХ 1 сорт ОКП 21 3221 0530 | РХ 2 сорт ОКП 21 3221 0540 | РД Высший сорт ОКП 21 3212 0320 | РД Первый сорт ОКП 21 3212 0330 |
|---|---|---|---|---|---|---|---|
| Внешний вид | Чешуирова- нная масса белого цвета. Допускается слабая окраска | Плавленая масса белого цвета. Допускается слабая окраска | Бесцветная прозрачная жидкость | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | Бесцветная или окрашенная жидкость. Допускается выкристалли- зованный осадок | |
| Массовая доля гидроксида натрия, %, не менее | 98,5 | 94,0 | 42,0 | 45,5 | 43,0 | 46,0 | 44,0 |
| Наименование предприятия | 2005 г. тыс.тонн | 2006 г. тыс.тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Стерлитамак | 239 | 249 | 20 | 20 |
| ОАО «Каустик» , Волгоград | 210 | 216 | 18 | 18 |
| ОАО «Саянскхимпласт» | 129 | 111 | 11 | 9 |
| ООО «Усольехимпром» | 84 | 99 | 7 | 8 |
| ОАО «Сибур-Нефтехим» | 87 | 92 | 7 | 8 |
| ОАО «Химпром» , Чебоксары | 82 | 92 | 7 | 8 |
| ВОАО «Химпром» , Волгоград | 87 | 90 | 7 | 7 |
| ЗАО «Илимхимпром» | 70 | 84 | 6 | 7 |
| ОАО «КЧХК» | 81 | 79 | 7 | 6 |
| НАК «АЗОТ» | 73 | 61 | 6 | 5 |
| ОАО «Химпром», Кемерово | 42 | 44 | 4 | 4 |
| Итого: | 1184 | 1217 | 100 | 100 |
| Наименование предприятия | 2005 г. тонн | 2006 г. тонн | доля в 2005 г.% | доля в 2006 г.% |
|---|---|---|---|---|
| ОАО «Каустик» , Волгоград | 67504 | 63510 | 62 | 60 |
| ОАО «Каустик» , Стерлитамак | 34105 | 34761 | 31 | 33 |
| ОАО «Сибур-Нефтехим» | 1279 | 833 | 1 | 1 |
| ВОАО «Химпром» , Волгоград | 5768 | 7115 | 5 | 7 |
| Итого: | 108565 | 106219 | 100 | 100 |






