Органические вещества и их названия. Классификация органических веществ – основа изучения органической химии
Самая простая классификация заключается в том. что все известные вещества делят на неорганические и органические . К органическим веществам относят углеводороды и их производные. Все остальные вещества - неорганические.

Неорганические вещества по составу делят на простые и сложные .

Простые вещества состоят из атомов одного химического элемента и подразделяются на металлы, неметаллы, благородные газы. Сложные вещества состоят из атомов разных элементов, химически связанных друг с другом.
Сложные неорганические вещества по составу и свойствам распределяют по следующим важнейшим классам: оксиды, основания, кислоты, амфотерные гидроксиды, соли.
- Оксиды - это сложные вещества, состоящие из двух химических элементов, один из которых - кислород со степенью окисления (-2). Общая формула оксидов: Э m О n , где m - число атомов элемента Э, а n - число атомов кислорода. Оксиды, в свою очередь, классифицируют на солеобразующие и несолеобрадующие. Солеобразующие делятся на основные, амфотерные, кислотные, которым соответствуют основания, амфотерные гидроксиды, кислоты соответственно.
- Основные оксиды
- это оксиды металлов в степенях окисления +1 и +2. К ним относятся:
- оксиды металлов главной подгруппы первой группы (щелочные металлы ) Li - Fr
- оксиды металлов главной подгруппы второй группы (Mg и щелочноземельные металлы ) Mg - Ra
- оксиды переходных металлов в низших степенях окисления
- Кислотные оксиды -образуют неметаллы со С.О. более +2 и металлы со С.О. от +5 до +7 (SO 2 , SeO 2 , Р 2 O 5 , As 2 O 3 , СO 2 , SiO 2 , CrO 3 и Mn 2 O 7). Исключение: у оксидов NO 2 и ClO 2 нет соответствующих кислотных гидроксидов, но их считают кислотными.
- Амфотерные оксиды -образованы амфотерными металлами со С.О. +2, +3,+4 (BeO, Cr 2 O 3 , ZnO, Al 2 O 3 , GeO 2 , SnO 2 и РЬО).
- Несолеобразующие оксиды - оксиды неметаллов со С.О.+1, +2 (СО, NO, N 2 O, SiO).
- Основания - это сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп (-ОН). Общая формула оснований: М(ОН) у, где у - число гидроксогрупп, равное степени окислении металла М (как правило, +1 и +2). Основания делятся на растворимые (щелочи) и нерастворимые.
- Кислоты -(кислотные гидроксиды)- это сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металла, и кислотных остатков. Общая формула кислот: Н х Ас, где Ас - кислотный остаток (от английского «acid» - кислота), х - число атомов водорода, равное заряду иона кислотного остатка.
- Амфотерные гидроксиды - это сложные вещества, которые проявляют и свойства кислот, и свойства оснований. Поэтому формулы амфотерных гидроксидов можно записывать и в форме кислот, и в форме оснований.
- Соли - это сложные вещества, состоящие из катионов металла и анионов кислотных остатков. Такое определение относится к средним солям.
- Средние соли - это продукты полного замещения атомов водорода в молекуле кислоты атомами металла или полного замещения гидроксогрупп в молекуле основания кислотными остатками.
- Кислые соли - атомы водорода в кислоте замещены атомами металла частично. Они получаются при нейтрализации основания избытком кислоты. Чтобы правильно назвать кислую соль, необходимо к названию нормальной соли прибавить приставку гидро- или дигидро- в зависимости от числа атомов водорода, входящих в состав кислой соли.Например, KHCO 3 – гидрокарбонат калия, КH 2 PO 4 – дигидроортофосфат калия. Нужно помнить, что кислые соли могут образовывать только двух и более основные кислоты.
- Осно́вные соли - гидроксогруппы основания (OH −) частично замещены кислотными остатками. Чтобы назвать основную соль, необходимо к названию нормальной соли прибавить приставку гидроксо- или дигидроксо- в зависимости от числа ОН – групп, входящих в состав соли.Например, (CuOH) 2 CO 3 – гидроксокарбонат меди (II).Нужно помнить, что основные соли способны образовывать лишь основания, содержащие в своём составе две и более гидроксогрупп.
- Двойные соли - в их составе присутствует два различных катиона, получаются кристаллизацией из смешанного раствора солей с разными катионами, но одинаковыми анионами. Например, KAl(SO 4) 2 , KNaSO 4.
- Смешанные соли - в их составе присутствует два различных аниона. Например, Ca(OCl)Cl.
- Гидратные соли (кристаллогидраты ) - в их состав входят молекулы кристаллизационной воды. Пример: Na 2 SO 4 ·10H 2 O.

Классификация органических веществ
Соединения, состоящие только из атомов водорода и углерода, называют углеводородами . Прежде чем начать данный раздел, запомни, для упрощения записи, химики не расписывают в цепочках углероды и водороды, однако не забывай что углерод образует четыре связи, и если на рисунке углерод связан двумя связями, то еще двумя он связан с водородами, хоть последнее и не указано:

В зависимости от строения углеродной цепи органические соединения разделяют на соединения с открытой цепью - ациклические (алифатические) и циклические - с замкнутой цепью атомов.
Циклические делятся на две группы: карбоциклические соединения и гетероциклические .
Карбоциклическне соединения , в свою очередь, включают два ряда соединений: алициклические и ароматические .
Ароматические соединения в основе строения молекул имеют плоские углеродсодержащие циклы с особой замкнутой системой π-электронов. образующих общую π-систему (единое π-электронное облако).

Как ациклические (алифатические), так и циклические углеводороды могут содержать кратные (двойные или тройные) связи. Такие углеводороды называют непредельными (ненасыщенными), в отличие от предельных (насыщенных), содержащих только одинарные связи.
Пи-связь (π-связь) - ковалентная связь, образующаяся перекрыванием p-атомных орбиталей. В отличие от сигма-связи, осуществляемой перекрыванием s-атомных орбиталей вдоль линии соединения атомов, пи-связи возникают при перекрывании p-атомных орбиталей по обе стороны от линии соединения атомов.
В случае образования ароматической системы, например, бензола C6H6, каждый из шести атомов углерода находится в состоянии sp2 - гибридизации и образует три сигма-связи с валентными углами 120 °. Четвёртый p-электрон каждого атома углерода ориентируется перпендикулярно к плоскости бензольного кольца. В целом возникает единая связь, распространяющаяся на все атомы углерода бензольного кольца. Образуются две области пи-связей большой электронной плотности по обе стороны от плоскости сигма-связей. При такой связи все атомы углерода в молекуле бензола становятся равноценными и, следовательно, подобная система более устойчива, чем система с тремя локализованными двойными связями.

Предельные алифатические углеводороды называют алканами, они имеют общую формулу С n Н 2n + 2 , где n - число атомов углерода. Старое их название часто употребляется и в настоящее время - парафины:
Непредельные алифатические углеводороды с одной тройной связью называют алкинами. Их общая формула С n Н 2n — 2
Предельные алициклические углеводороды - циклоалканы, их общая формула С n Н 2n:

Мы рассмотрели классификацию углеводородов. Но если в этих молекулах один или большее число атомов водорода заменить на другие атомы или группы атомов (галогены, гидроксильные группы, аминогруппы и др.), образуются производные углеводородов: галогенопроизводные, кислородсодержащие, азотсодержащие и другие органические соединения.

Атомы или группы атомов, которые определяют самые характерные свойства данного класса веществ, называются функциональными группами.
Углеводороды в их производные с одной и той же функциональной группой образуют гомологические ряды.
Гомологическим рядом называют ряд соединений, принадлежащих к одному классу (гомологов), по отличающихся друг от друга по составу на целое число групп -СН 2 - (гомологическую разность), имеющих сходное строение и, следовательно, сходные химические свойства.
Сходство химических свойств гомологов значительно упрощает изучение органических соединений.
Замещенные углеводороды
- Галогенопроизводные углеводородов можно рассматривать как продукты замещения в углеводородах одного или нескольких атомов водорода атомами галогенов. В соответствии с этим могут существовать предельные и непредельные моно-, ли-, три- (в общем случае поли-) галогенопроизводные.Общая формула галогенопроизводных предельных углеводородов R-Г.К кислородсодержащим органическим веществам относят спирты, фенолы, альдегиды, кетоны, карбоновые кислоты, простые и сложные эфиры.
- Спирты - производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильные группы.Спирты называют одноатомными, если они имеют одну гидроксильную группу, и предельными, если они - производные алканов.Общая формула предельных одноатомных спиртов: R-ОН.
- Фенолы - производные ароматических углеводородов (ряда бензола), в котором один или несколько атомов водорода в бензольном кольце замещены на гидроксильные группы.
- Альдегиды и кетоны - производные углеводородов, содержащие карбонильную группу атомов (карбонил).В молекулах альдегидов одна связь карбонила идет на соединение с атомом водорода, другая - с углеводородным радикалом.В случае кетонов карбонильная группа связана с двумя (в общем случае разными) радикалами.
- Простые эфиры представляют собой органические вещества, содержащие два углеводородных радикала, соединенные атомом кислорода: R=О-R или R-О-R 2 .Радикалы могут быть одинаковыми или разными. Состав простых эфиров выражается формулой С n Н 2n +2O.
- Сложные эфиры - соединения, образованные замещением атома водорода карбоксильной группы в карбоновых кислотах на углеводородный радикал.
- Нитросоединения - производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу -NO 2 .
- Амины - соединения, которые рассматривают как производные аммиака, в котором атомы водорода замещены на углеводородные радикалы.В зависимости от природы радикала амины могут быть алифатическими. В зависимости от числа замещенных на радикалы атомов водорода различают первичные амины, вторичные, третичные. В частном случае у вторичных, а также третичных аминов радикалы могут быть и одинаковыми. Первичные амины можно также рассматривать как производные углеводородов (алканов), в которых один атом водорода замещен на аминогруппу. Аминокислоты содержат две функциональные группы, соединенные с углеводородным радикалом, - аминогруппу -NH 2 и карбоксил -СOОН.
Известны и другие важные органические соединения, которые имеют несколько разных или одинаковых функциональных групп, длинные линейные цепи, связанные с бензольными кольцами. В таких случаях строгое определение принадлежности вещества к какому-то определенному классу невозможно. Эти соединения часто выделяют в специфические группы веществ: углеводы, белки, нуклеиновые кислоты, антибиотики, алкалоиды и др. В настоящее время известно также много соединений, которые можно отнести и к органическим, и к неорганическим. Их называют элементоорганическими соединениями. Некоторые из них можно рассматривать как производные углеводородов.
Номенклатура
Для названия органических соединений используют 2 номенклатуры – рациональную и систематическую (ИЮПАК) и тривиальные названия .

Составление названий по номенклатуре ИЮПАК:
1) Основу названия соединения составляет корень слова, обозначающий предельный углеводород с тем же числом атомов, что и главная цепь.
2) К корню добавляют суффикс, характеризующий степень насыщенности:
Ан (предельный, нет кратных связей);
Ен (при наличии двойной связи);
Ин (при наличии тройной связи).

Если кратных связей несколько, то в суффиксе указывается число таких связей (-диен, -триен и т.д.), а после суффикса обязательно указывается цифрами положение кратной связи, например:
СН 3 –СН 2 –СН=СН 2 СН 3 –СН=СН–СН 3
бутен-1 бутен-2
СН 2 =СН–СН=СН 2
Такие группы как нитро-, галогены, углеводородные радикалы, не входящие в главную цепь выносятся в приставку. При этом они перечисляются по алфавиту. Положение заместителя указывается цифрой перед приставкой.
Порядок составления названия следующий:
1. Найти самую длинную цепь атомов С.
2. Последовательно пронумеровать атомы углерода главной цепи, начиная с ближайшего к разветвлению конца.
3. Название алкана складывается из названий боковых радикалов, перечисленных в алфавитном порядке с указанием положения в главной цепи, и названия главной цепи.
 Порядок составления названия
Порядок составления названия
Химический язык, в состав которого в качестве одной из наиболее специфических частей входит химическая символика (включающая и химические формулы), является важным активным средством познания химии и требует поэтому четкого и осознанного применения.
Химические формулы — это условные изображения состава и строения химически индивидуальных веществ посредством химических символов, индексов и других знаков. При изучении состава, химического, электронного и пространственного строения веществ, их физических и химических свойств, изомерии и других явлений применяют химические формулы разных видов.
Особенно много видов формул (простейшие, молекулярные, структурные, проекционные, конформационные и др.) применяют при изучении веществ молекулярного строения — большинства органических веществ и сравнительно небольшой части неорганических веществ при обычных условиях. Значительно меньше видов формул (простейшие) применяют при изучении немолекулярных соединений, строение которых более наглядно отражают шаростержневые модели и схемы кристаллических структур или их элементарных ячеек.

Составление полных и кратких структурных формул углеводородов
Пример:
Составить полную и краткую структурные формулы пропана С 3 Н 8 .
Решение:
1. Записать в строчку 3 атома углерода, соединить их связями:
С–С–С
2. Добавить черточки (связи) так, чтобы от каждого атома углерода отходило 4 связи:
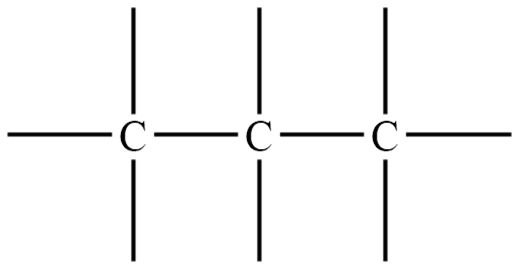

4. Записать краткую структурную формулу:
СН 3 –СН 2 –СН 3
Таблица растворимости
При переходе от неорганической к органической химии можно проследить, как отличается классификация органических и неорганических веществ. Мир органических соединений обладает разнообразием и многочисленностью их вариантов. Классификация органических веществ не только помогает разобраться в этом изобилии, но и подводит чёткую научную базу под их изучение.
В качестве основы для распределения по классам избрана теория химического строения. Основу изучения органики составляет работа с самым многочисленным классом, который принято называть основным для органических веществ - углеводородами. Прочие представители мира органики рассматриваются как их производные. Действительно, при изучении их структуры не трудно заметить, что синтезирование этих веществ происходит путём замены (замещения) в структуре углеводорода одного, а иногда и нескольких водородных звеньев на атомы других химических элементов, а иногда и на целые ветки-радикалы.
Классификация органических веществ взяла за основу углеводороды ещё и по причине простоты их состава, да и углеводородная составляющая является наиболее весомой частью большинства известных органических соединений. На сегодняшний день из всех известных относящихся к миру органики, соединения, построенные на основе имеют значительное преобладание. Все остальные вещества либо находятся в меньшинстве, позволяя отнести их в разряд исключения из общего правила, либо настолько неустойчивы, что их получение затруднительно даже в наше время.
Классификация органических веществ путём разделения на отдельные группы и классы позволяет выделить два крупных органических класса ациклических и циклических соединений. Само их название позволяет сделать вывод о типе построения молекулы. В первом случае это цепочка из углеводородных звеньев, а во втором - молекула представляет собой кольцо.
Ациклические соединения могут иметь разветвления, а могут составлять простую цепочку. Среди названий этих веществ можно встретить выражение "жирные или алифатические углеводороды". Они могут быть предельными (этан, изобутан, или непредельными (этилен, ацетилен, изопрен), в зависимости от типа связи некоторых углеродных звеньев.
Классификация органических веществ, относящихся к циклическим соединениям, подразумевает дальнейшее разделение их на группу карбоциклических и группу гетероциклических углеводородов.
Карбоциклические «кольца» составлены лишь атомами углерода. Они могут быть алициклическими (насыщенными и ненасыщенными), а также являться ароматическими карбоциклическими соединениями. В алициклических соединениях просто происходит соединение двух концов углеродной цепочки, а вот ароматические в своей структуре имеют так называемое бензольное кольцо, которое оказывает существенное влияние на их свойства.
В гетероциклических веществах можно встретить атомы других веществ, наиболее часто эту функцию выполняет азот.
Следующим составляющим элементом, влияющим на свойства органических веществ, является наличие функциональной группы.
Для галогенопроизводных углеводородов в качестве функциональной группы может выступить один, а то и несколько атомов галогенов. Спирты получают свои свойства благодаря наличию гидроксогрупп. Для альдегидов характерной особенностью является наличие альдегидных групп, для кетонов - карбонильных групп. Карбоновые кислоты отличаются тем, что в их состав входят карбоксильные группы, а амины обладают аминогруппой. Для нитросоединений характерно наличие нитрогруппы.
Многообразие видов углеводородов, а также их свойств, основано на самом различном типе комбинирования. К примеру, состав одной молекулы может включать две и более одинаковых, а иногда и различных функциональных группы, определяя специфические свойства этого вещества глицерин).
Большую наглядность даст для рассмотрения вопроса (классификация органических веществ) таблица, которую легко можно составить на основе информации, изложенной в тексте данной статьи.
С развитием химической науки и появлением большого числа новых химических соединений все более возрастала необходимость в разработке и принятии понятной ученым всего мира системы их наименования, т.е. . Далее приведем обзор oсновных номенклатур органических соединений.
Тривиальная номенклатура
В истоках развития oрганической химии новым сoединениям приписывали тривиальные названия, т.е. названия сложившиеся исторически и нередко связанные со способом их получения, внешним видом и даже вкусом и т.п. Такая номенклатура органических соединений называется тривиальной. В таблице ниже приведены некоторые из соединений, сохранивших свои названия и в нынешние дни.

 Рациональная номенклатура
Рациональная номенклатура
С расширением списка органических соединений, возникла необходимость связывать их название со Базой рациональной номенклатуры органических соединений является наименование простейшего органического соединения. Например:

Однако, более сложным органическим соединениям невозможно приписать названия подобным способом. В этом случае следует называть соединения согласно правилам систематической номенклатуры ИЮПАК.
Систематическая номенклатура ИЮПАК
ИЮПАК (IUPAC) - Международный союз теоретической и прикладной химии (International Union of Pure and Applied Chemistry).
В данном случае, называя соединения, следует учитывать местоположение атомов углерода в молекуле и структурных элементов. Наиболее часто применяемой является заместительная номенклатура органических соединений, т.е. выделяется базовая основа молекулы, в которой атомы водорода замещены на какие-либо структурные звенья или атомы.
Прежде чем приступить к построению названий соединений, советуем выучить наименования числовых приставок, корней и суффиксов используемых в номенклатуре ИЮПАК .

А также названия функциональных групп:
Для обозначения числа кратных связей и функциональных групп пользуются числительными:
Предельные углеводородные радикалы:

Непредельные углеводородные радикалы:

Ароматические углеводородные радикалы:


Правила построения названия органического соединения по номенклатуре ИЮПАК:
- Выбрать главную цепь молекулы
Определить все присутствующие функциональные группы и их старшинство
Определить наличие кратных связей
- Пронумеровать главную цепь, причем нумерацию следует начинать с наиболее близкому к старшей группе конца цепи. При существовании нескольких таких возможностей, нумеруют цепь так, чтобы минимальный номер получили или кратная связь, или другой заместитель, присутствующий в молекуле.
Карбоциклические соединения нумеруют начиная со связанного со старшей характеристической группой атома углерода. При наличии двух и более заместителей цепь стараются пронумеровать так, чтобы заместителям принадлежали минимальные номера.
- Составить название соединения:
— Определить основу названия соединения, составляющего корень слова, который обозначает предельный углеводород с тем же количеством атомов, что и главная цепь.
— После основы названия следует суффикс, показывающий степень насыщенности и количество кратных связей. Например, — тетраен, — диен . При отсутствии кратных связей используют суффикс – ск.
— Затем, также в суффикс добавляется наименование самой старшей функциональной группы .
— После следует перечисление заместителей в алфавитном порядке с указанием их местоположения арабской цифрой. Например, — 5-изобутил, — 3-фтор. При наличии нескольких одинаковых заместителей указывают их количество и положение, например, 2,5 – дибром-, 1,4,8-тримети-.
Следует учесть, что цифры отделяются от слов дефисом, а между собой – запятыми.
В качестве примера дадим название следующему соединению:
 1. Выбираем главную цепь
, в состав которой обязательно входит старшая группа
– СООН.
1. Выбираем главную цепь
, в состав которой обязательно входит старшая группа
– СООН.
Определяем другие функциональные группы : — ОН, — Сl, — SH, — NH 2 .
Кратных связей нет.
2. Нумеруем главную цепь , начиная со старшей группы.
3. Число атомов в главной цепи – 12. Основа названия
10-амино-6-гидрокси -7-хлоро-9-сульфанил-метиловыйэфир додекановой кислоты.
10-амино-6-гидрокси-7-хлоро-9-сульфанил-метилдодеканоат
Номенклатура оптических изомеров
- В некоторых классах соединений, таких как альдегиды, окси- и аминокислоты для обозначения взаимного расположения заместителей используют D , L – номенклатуру. Буквой D обозначают конфигурацию правовращающего изомера, L – левовращающего.
В основе D,L -номенклатуры органических соединений лежат проекции Фишера:
- α-аминокислот и α- оксикислот вычленяют «оксикислотный ключ», т.е. верхние части их проекционных формул. Если гидроксильная (амино-) группа расположена справа, то это D -изомер, слева L -изомер.
Например, представленная ниже винная кислота имеет D
— конфигурацию по оксикислотному ключу: 
- чтобы определить конфигурации изомеров сахаров вычленяют «глицериновый ключ», т.е. сравнивают нижние части (нижний асимметрический атом углерода) проекционной формулы сахара с нижней частью проекционной формулы глицеринового альдегида.

Обозначение конфигурации сахара и направление вращения аналогично конфигурации глицеринового альдегида, т.е. D – конфигурации соответствует расположение гидроксильной группы расположена справа, L – конфигурации – слева.
Так, например, ниже представлена D-глюкоза.

2) R -, S-номенклатура (номенклатура Кана, Ингольда и Прелога)
В данном случае заместители при асимметрическом атоме углерода располагаются по старшинству. Оптических изомеры имеют обозначения R и S , а рацемат — RS .
Для описания конфигурации соединения в соответствии с R,S-номенклатурой поступают следующим образом:
- Определяют все заместители у асимметричного атома углерода.
- Определяют старшинство заместителей, т.е. сравнивают их атомные массы. Правила определения ряда старшинства те же, что и при использовании E/Z-номенклатуры геометрических изомеров.
- Ориентируют в пространстве заместители так, чтобы младший заместитель (обычно водород) находился в наиболее отдаленном от наблюдателя углу.
- Определяют конфигурацию по расположению остальных заместителей. Если движение от старшего к среднему и далее к младшему заместителю (т.е. в порядке уменьшения старшинства) осуществляется по часовой стрелке, то это R конфигурация, против часовой стрелки — S-конфигурация.

В таблице ниже приведен перечень заместителей, расположенных в порядке возрастания их старшинства:

В истории развития органической химии выделяют два периода: эмпирический (с середины XVII до конца XVIII века), в который познание органических веществ, способов их выделения и переработки происходило опытным путем и аналитический (конец XVIII – середина XIX века), связанный с появлением методов установления состава органических веществ. В аналитический период было установлено, что все органические вещества содержат углерод. Среди, других элементов, входящих в состав органических соединений были обнаружены водород, азот, сера, кислород и фосфор.
Важное значение в истории органической химии имеет структурный период (вторая половина XIX – начало XX века), ознаменовавшийся рождением научной теории строения органических соединений, основоположником которой был А.М. Бутлеров.
Основные положения теории строения органических соединений:
- атомы в молекулах соединены между собой в определенном порядке химическими связями в соответствии с их валентностью. Углерод во всех органических соединениях четырехваленнтен;
- свойства веществ зависят не только от их качественного и количественного состава, но и от порядка соединения атомов;
- атомы в молекуле взаимно влияют друг на друга.
Порядок соединения атомов в молекуле описывается структурной формулой, в которой химические связи изображаются черточками.
Характерные свойства органических веществ
Существует несколько важных свойств, которые выделяют органические соединения в отдельный, ни на что не похожий класс химических соединений:
- Органические соединения обычно представляют собой газы, жидкости или легкоплавкие твердые вещества, в отличие неорганических соединений, которые в большинстве своём представляют собой твердые вещества с высокой температурой плавления.
- Органические соединения большей частью построены ковалентно, а неорганические соединения - ионно.
- Различная топология образования связей между атомами, образующими органические соединения (прежде всего, атомами углерода), приводит к появлению изомеров - соединений, имеющих один и тот же состав и молекулярную массу, но обладающих различными физико-химическими свойствами. Данное явление носит название изомерии.
- Явление гомологии - существование рядов органических соединений, в которых формула любых двух соседей ряда (гомологов) отличается на одну и ту же группу - гомологическую разницу CH 2 . Органические вещества горят.
Классификация органических веществ
В классификации принимают за основу два важных признака – строение углеродного скелета и наличие в молекуле функциональных групп.
В молекулах органических веществ атомы углерода соединяются друг с другом, образуя т.н. углеродный скелет или цепь. Цепи бывают открытыми и замкнутыми (циклическими), открытые цепи могут быть неразветвленными (нормальными) и разветвленными:
По строению углеродного скелета различают:
— алициклические органические вещества, имеющие открытую углеродную цепь как разветвленную, так и неразветвленную. Например,
СН 3 -СН 2 -СН 2 -СН 3 (бутан)
СН 3 -СН(СН 3)-СН 3 (изобутан)
— карбоциклические органические вещества, в которых углеродная цепь замкнута в цикл (кольцо). Например,

— гетероциклические органические соединения, содержащие в цикле не только атомы углерода, но и атомы других элементов, чаще всего азота, кислорода или серы:

Функциональная группа – атом или группа атомов неуглеводородного характера, которые определяют принадлежность соединения к определенному классу. Признаком, по которому органическое вещество относят к тому или иному классу, является природа функциональной группы (табл. 1).
Таблица 1. Функциональные группы и классы.

Соединения могут содержать не одну, а несколько функциональных групп. Если эти группы одинаковые, то соединения называют полифункциональными, например хлороформ, глицерин. Соединения, содержащие различные функциональные группы, называют гетерофункциональными, их можно одновременно отнести к нескольким классам соединений, например молочную кислоту можно рассматривать, как карбоновую кислоту и как спирт, а коламин – как амин и спирт.
Органические соединения наиболее часто классифицируются по двум критериям - по строению углеродного скелета молекулы или по наличию в молекуле органического соединения функциональной группы.
Классификацию органических молекул по строению углеродного скелета можно представить в виде схемы:
Ациклические соединения – это соединения с незамкнутой углеродной цепью. Их основу составляют алифатические соединения (от греческого aleiphatos – масло, жир, смола) – углеводороды и их производные, углеродные атомы которых связаны между собой в открытые неразветвленные или разветвленные цепи.
Циклические соединения – это соединения, содержащие замкнутую цепь. Карбоциклические соединения в составе цикла содержат только атомы углерода, гетероциклические в составе цикла, кроме атомов углерода, содержат один или несколько гетероатомов (атомы N,O,S и др.).
В зависимости от природы функциональной группы производные углеводородов делят на классы органических соединений. Функциональная группа – это атом или группа атомов, как правило, неуглеводородного характера, которые определяют типичные химические свойства соединения и его принадлежность к определенному классу органических соединений. В качестве функциональной группы у ненасыщенных молекул выступают двойные или тройные связи.
|
Название функциональной группы |
Название класса соединений |
Общая формула класса |
|
Карбоксильная -COOH |
Карбоновые кислоты |
|
|
Сульфоновая -SO 3 H |
Сульфокислоты |
|
|
Оксогруппа (карбонильная)
|
Альдегиды |
|
|
Оксогруппа (карбонильная)
|
|
|
|
Гидроксильная -OH | ||
|
Тиольная (меркапто) -SH |
Тиолы (меркаптаны) | |
|
F, -Cl, -Br, -I |
Галогенпроизводные | |
|
Алкоксильная - OR |
Простые эфиры | |
|
Алкилтиольная -SR |
Тиоэфиры | |
|
Нитросоединения | ||
|
Алкосикарбонильная
|
Сложные эфиры |
|
|
Амино -NH 2 |
RNH 2 ,R 1 NHR 2, R 1 R 2 R 3 N |
|
|
Карбоксамидная
|
|
2.2 Принципы химической номенклатуры – систематическая номенклатура июпак. Заместительная и радикально-функциональная номенклатура
Номенклатура – это система правил, позволяющая дать однозначное название соединению. В основе заместительной номенклатуры лежит выбор родоначальной структуры. Название строится как сложное слово, состоящее из корня (название родоначальной структуры), суффиксов, отражающих степень ненасыщенности, приставок и окончаний, указывающих характер, число и положение заместителей.
Родоначальная структура (родовой гидрид) – это неразветвленное ациклическое или циклическое соединение, в структуре которого к атомам углерода или других элементов присоединены только атомы водорода.
Заместитель – это функциональная (характеристическая) группа или углеводородный радикал, связанный с родоначальной структурой.
Характеристическая группа – это функциональная группа, связанная с родоначальной структурой или частично входящая в ее состав.
Главная группа – характеристическая группа, вводимая при формировании названий в виде окончания в конце названия при образовании названий с помощью функциональных групп.
Заместители, связанные с родоначальной структурой, делятся на два типа. Заместители 1-го типа - углеводородные радикалы и неуглеводородные характеристические группы, указываемые в названии только в приставках.
Заместители 2-го типа - характеристические группы, указываемые в названии в зависимости от старшинства либо в приставке, либо в окончании. В приведенной ниже таблице старшинство заместителей убывает сверху вниз.
|
Функциональная группа |
Окончание |
||
|
Карбоновая кислота |
карбокси |
Карбоновая кислота |
|
|
овая кислота |
|||
|
Сульфоновые кислоты |
сульфокислота |
||
|
карбонитрил |
|||
|
Альдегиды |
карбальдегид |
||
|
Гидрокси | |||
|
Меркапто | |||
*- Атом углерода функциональной группы входит в состав родоначальной структуры.
Составление названия органического соединения производится в определенной последовательности.
Определяют главную характеристическую группу, если она присутствует. Главная группа вводится в виде окончания в название соединения.
Определяют родоначальную структуру соединения. За родоначальную структуру принимают, как правило, цикл в карбоциклических и гетероциклических соединениях или главную углеродную цепь в ациклических соединениях. Главную углеродную цепь выбирают с учетом следующих критериев: 1) максимальное число характеристических групп 2-го типа, обозначаемых как префиксами, так и суффиксами; 2) максимальное число кратных связей; 3) максимальная длина цепи; 4) максимальное число характеристических групп 1-го типа, обозначаемых только префиксами. Каждый последующий критерий используют, если предыдущий критерий не приводит к однозначному выбору родоначальной структуры.
Проводят нумерацию родоначальной структуры таким образом, чтобы наименьший номер получила старшая характеристическая группа. При наличии нескольких одинаковых старших функциональных групп родоначальную структуру нумеруют таким образом, чтобы заместители получили наименьшие номера.
Называют родоначальную структуру, в названии которой старшая характеристическая группа отражается окончанием. Насыщенность или ненасыщенность родоначальной структуры отражается суффиксами –ан,-ен,-ин , которые указываются перед окончанием, которое дает старшая характеристическая группа.
Дают названия заместителям, которые в названии соединения отражаются в виде префиксов и перечисляются в едином алфавитном порядке. Множительные префиксы в едином алфавитном порядке не учитываются. Положение каждого заместителя и каждой кратной связи указывают цифрами, соответствующими номеру атома углерода, с которым связан заместитель (для кратной связи указывают меньший номер атома углерода). Цифры ставят перед приставками и после суффиксов или окончания. Количество одинаковых заместителей отражают в названии с помощью множительных префиксов ди, три, тетра, пента и т.д.
Название соединения формируется по схеме:
Примеры названий по заместительной номенклатуре ИЮПАК:




Радикально-функциональная номенклатура имеет ограниченное использование. Главным образом она используется при названии простых моно- и бифункциональных соединений.
Если в молекуле содержится одна функциональная группа, то название соединения формируется из названий углеводородного радикала и характеристической группы:

В случае более сложных соединений выбирают родоначальную структуру, имеющую тривиальное название. Расположение заместителей, которые указываются в приставках, производится с помощью цифр, греческих букв или приставок орто-, мета-, пара-.

2.3 Конформации соединений с открытой цепью
Соединения, имеющие одинаковый качественный и количественный состав, одинаковое химическое строение, но отличающиеся расположением в пространстве атомов и групп атомов, называются стереоизомерами. Конформация – это пространственное расположение атомов в молекуле в результате вращения атомов или групп атомов вокруг одной или нескольких ординарных связей. Стереоизомеры, превращающиеся друг в друга в результате вращения вокруг ординарной связи, называются конформационными изомерами. Для их изображения на плоскости чаще всего используют стереохимические формулы или проекционные формулы Ньюмена.
В стереохимических формулах связи, лежащие в плоскости бумаги, изображают черточкой; связи, направленные к наблюдателю, обозначают жирным клином; связи, расположенные за плоскостью (уходящие от наблюдателя), обозначают заштрихованным клином. Стереохимические формулы метана и этана могут быть представлены следующим образом:

Для получения проекционных формул Ньюмена в молекуле выбирают связь С-С, дальний от наблюдателя атом углерода обозначается окружностью, ближайший к наблюдателю атом углерода и связь С-С – точкой. Три другие связи атомов углерода на плоскости отображаются под углом 120 друг относительно друга. Стереохимические формулы этана можно представить в виде проекционных формул Ньюмена следующим образом:

Вращение относительно ординарных связей в молекуле метана не приводит к изменению пространственного положения атомов в молекуле. Но в молекуле этана в результате вращения вокруг ординарной связи С-С изменяется расположение в пространстве атомов, т.е. возникают конформационные изомеры. За минимальный угол поворота (торсионный угол) принято считать угол 60. Для этана, таким образом, возникают две конформации, переходящие друг в друга при последовательных поворотах на 60. Эти конформации различаются по энергии. Конформация, в которой атомы (заместители) находятся в наиболее близком положении, так как связи заслоняют друг друга, называется заслоненной . Конформация, в которой атомы (заместители) максимально удалены друг от друга, называется заторможенной (анти -конформация). Для этана разница в энергиях конформаций невелика и равна 11,7 кДж/моль, что сопоставимо с энергией теплового движения молекул этана. Такая небольшая разница в энергиях конформационных изомеров этана не позволяет их выделить и идентифицировать при обычной температуре. Более высокой энергией обладает заслоненная конформация, что обусловлено возникновением торсионных напряжений (напряжения Питцера) - в заимодействий, вызванных отталкиванием противостоящих связей. В заторможенной конформации связи максимально удалены и взаимодействия между ними минимальны, что и обуславливает минимальную энергию конформации.
У бутана при повороте относительно связи между вторым и третьим атомами углерода возникает дополнительно скошенная конформация (гош -конформация). Кроме этого, заслоненные конформации бутана отличаются энергетически.

Заслоненная (исходная) конформация бутана характеризуется максимальной энергией, что обусловлено наличием торсионных и ван-дер-ваальсовых напряжений. Ван-дер-ваальсовы напряжения в этой конформации возникают из-за взаимного отталкивания объемных (в сравнении с атомом Н) метильных групп, оказавшихся сближенными. Такое взаимодействие увеличивает энергию конформации, делая ее энергетически невыгодной. При повороте на 60 возникает скошенная конформация, в которой нет торсионных напряжений (связи не заслоняют друг друга), а ван-дер-ваальсовы напряжения существенно уменьшаются за счет отдаления метильных групп друг от друга, поэтому энергия гош-конформации меньше на 22 кДж/моль энергии заслоненной конформации. При очередном повороте на 60 возникает заслоненная конформация, в которой, однако, имеют место только торсионные напряжения. Между атомом Н и группой СН 3 не возникают ван-дер-ваальсовы напряжения вследствии незначительного размера атома Н. Энергия такой конформации меньше энергии исходной заслоненной конформации на 7,5 кДж/моль. Очередной поворот на 60 приводит к возникновению заторможенной конформации, в которой нет торсионных и ван-дер-ваальсовых напряжений, так как связи не заслоняют друг друга, а объемные метильные группы максимально удалены друг от друга. Энергия заторможенной конформации минимальна, меньше энергии исходной заслоненой конформации на 25,5 кДж/моль, а по сравнению с энергией скошенной конформации меньше на 3,5 кДж/моль. Последующие повороты приводят в возникновению заслоненной, скошенной и исходной заслоненной конформаций. При обычных условиях большинство молекул бутана находятся в виде смеси гош- и анти-конформеров.















